Titratoren
-
Titratoren Kyoto Electronics AT-710BID-Nummer: 47541Versand: 4-6 WochenStatus: Anbieter1.430,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Titratoren Mettler Excellence T7ID-Nummer: 45887Versand: 4-6 WochenStatus: Anbieter49.300,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Titratoren Mettler Excellence T5ID-Nummer: 45069Versand: 10-14 WerktageStatus: Lagergerät11.600,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Titratoren Mettler Compact C30SID-Nummer: 45068Versand: 10-14 WerktageStatus: Lagergerät12.800,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Titratoren Metrohm 851 TitrandoID-Nummer: 44682Versand: 4-6 WochenStatus: Anbieter19.100,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Titratoren Metrohm Titrino 794ID-Nummer: 39932Versand: 10-14 WerktageStatus: Lagergerät3.900,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Top AngebotTitratoren Metrohm 670ID-Nummer: 33538Versand: 10-14 WerktageStatus: Lagergerät-15% Rabatt Sonderangebot 472,60 € Normalpreis 556,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Top AngebotTitratoren Thermo ORION 960ID-Nummer: 32795Versand: 10-14 WerktageStatus: Lagergerät-30% Rabatt Sonderangebot 2.621,50 € Normalpreis 3.745,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Titratoren Metrohm 848 Titrando Plus Titrator 801 Stirrer PriID-Nummer: 72764Versand: 4-6 WochenStatus: Labprocure5.940,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Titratoren Metrohm 836 Titrando 803 Ti Stand 801 Stirrer 800ID-Nummer: 72742Versand: 4-6 WochenStatus: Labprocure6.615,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Titratoren Metrohm 831 mit Rührer 821 und ThermodruckerID-Nummer: 72691Versand: 10-14 WerktageStatus: Labprocure5.130,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Titratoren Terumo TSCD-II Sterile Tubing WelderTerumo TSCD-IIID-Nummer: 72683Versand: 4-6 WochenStatus: Labprocure6.203,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Titratoren ABB Group PowerScale Uninterruptible Power SupplyAID-Nummer: 72682Versand: 4-6 WochenStatus: Labprocure5.332,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Titratoren Büchi B-191 Mini Spray DryerBüchi B-191 Mini SprayID-Nummer: 71819Versand: 4-6 WochenStatus: Labprocure17.482,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Titratoren Ismatec IPS mit Pumpenkopf PTFE-DiaphragmID-Nummer: 71567Versand: 4-6 WochenStatus: Labprocure2.835,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Titratoren Thermo VisionMateHigh Speed 2D Barcode ReaderThermID-Nummer: 71443Versand: 4-6 WochenStatus: Labprocure8.775,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Titratoren Foss Kjeltec 2200 Auto Distillation UnitFoss KjeltID-Nummer: 70433Versand: 4-6 WochenStatus: Labprocure6.074,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Titratoren Watson-Marlow Schlauchpumpe Modell Sci 323U/DID-Nummer: 62305Versand: 10-14 WerktageStatus: Labprocure3.780,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Titratoren Giussani Solar Portable Temperature CalibratorGiusID-Nummer: 62063Versand: 4-6 WochenStatus: Labprocure6.749,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Titratoren Oxoid Air SamplerOxoid Air SamplerID-Nummer: 61712Versand: 4-6 WochenStatus: Labprocure5.399,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Titratoren Metrohm 857 Titrando + 801 Stirrer + 800 Dosino 20ID-Nummer: 61489Versand: 4-6 WochenStatus: Labprocure5.400,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Titratoren Metrohm Probenwechsler 730 mit Schwenkarm 759ID-Nummer: 61227Versand: 4-6 WochenStatus: Labprocure3.780,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Titratoren Perkin Elmer Flex Drop Plus DispenserID-Nummer: 61082Versand: 4-6 WochenStatus: Labprocure31.200,00 €Exkl. 19% Steuern , exkl. Versandkosten
-
Titratoren Atlas Copco SF4 Oil-free CompressorAtlas Copco SF4ID-Nummer: 60135Versand: 4-6 WochenStatus: Labprocure6.743,00 €Exkl. 19% Steuern , exkl. Versandkosten
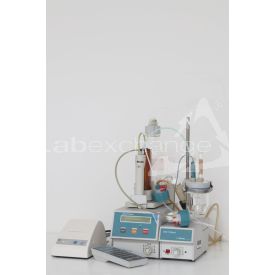
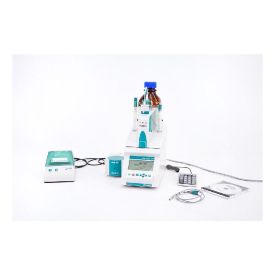
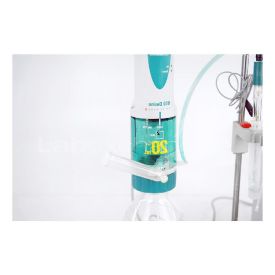
Ein Titrator wird in der Chemie zur quantitativen Analyse eingesetzt. Bei der Titration wird ein bekannter Stoff, mit unbekannter Konzentration, mit einer Maßlösung, deren Konzentration bekannt ist, umgesetzt. Das Volumen der verbrauchten Maßlösung wird gemessen. Anhand der Stöchiometrie kann bei der Titration auf die unbekannte Konzentration der Probelösung geschlossen werden.
Durchführung der Titration
Bei der Titration wird mit einer Bürette zur Probelösung, dem sogenannten Titrand, ein Reagenz bekannter Konzentration, der sogenannte Titrator oder Titrant, hinzu getropft, bis der Äquivalenzpunkt erreicht ist. Dieser lässt sich durch chemische und physikalische Methoden ermitteln. Das verbrauchte Volumen kann an der Bürette abgelesen werden. Bevor die eigentliche Titration beginnt, wird der Gehalt der Maßlösung genau bestimmt, und ein Korrekturfaktor, der Titer ermittelt, um die Genauigkeit der Messung zu erhöhen. Je nach chemischer Reaktion, lassen sich die Titrationen unterscheiden. Die Säure-Base Titration beruht auf der Säure-Base Reaktion. Durch Zugabe eines pH-Indikators lässt sich der Endpunkt bestimmen. Eine weitere Möglichkeit stellt die Messung des pH-Wertes anhand einer Elektrode dar. Nach Ermittlung des pH-Werts lässt sich bei der Säure-Base Titration die verbrauchte Maßlösung ermitteln. Eine andere Möglichkeit der Titration stellt die Fällungstitration dar. Ein Beispiel hierfür ist die Reaktion von Silberionen mit Chloridionen. Der Endpunkt ist durch die Bildung eines milchigen Niederschlages bestimmbar. Die Komplexometrische Titration beruht auf einer Komplexbildungsreaktion. Durch den Zusatz von Farbstoffen können die Farbänderungen durch Bildung eines Komplexes photometrisch verfolgt und folglich auch bestimmt werden. Ein typisches Beispiel für die komplexometrische Titration stellt die Titration mit EDTA (Ethylendiamintetraacetat) dar. Für die Titration kann auch auf die Redox-Reaktion, das heißt auf Verfahren wie die Manganometrie und die Cerimetrie, zurückgegriffen werden. Grundsätzlich gibt es zwei Arten von Titrationen. Die direkte und die indirekte Titration. Bei der direkten werden die Probelösung und die Reagenzlösung unmittelbar miteinander umgesetzt. Die Probelösung wird vorgeletzt und mit der Reagenzlösung direkt titriert. Bei der indirekten Titration wird der zu untersuchende Stoff vor der Titration in einer chemischen Reaktion umgesetzt. Hierbei wird dieser in einer chemischen Reaktion zu einem genau festgelegten anderen Stoff umgesetzt, der dann titrimetrisch bestimmt wird. Eine weitere Unterscheidung stellt die Rücktitration und die Substitutionstitration dar.
Literatur
•http://de.wikipedia.org/w/index.php?title=Titration&oldid=86735385 (Abgerufen: 29.03.11).
•http://www.seilnacht.com/Lexikon/Titratio.htm (Abgerufen: 29.03.11).
•http://de.wikipedia.org/w/index.php?title=S%C3%A4ure-Base-Titration&oldid=86694170 (Abgerufen: 29.03.11).